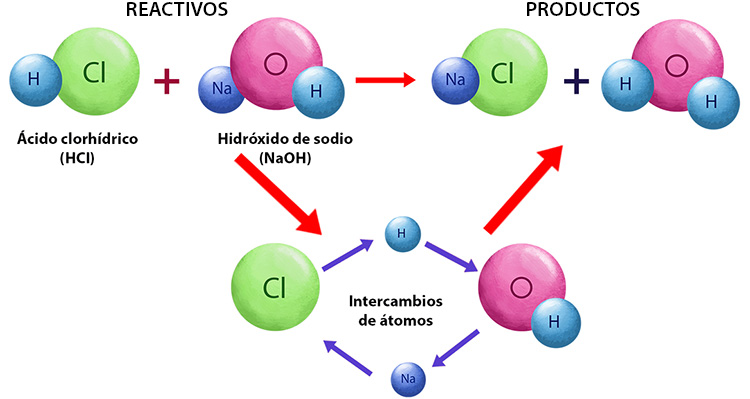
Las reacciones químicas son procesos en los cuales una o más sustancias (llamadas reactivos) se transforman en nuevas sustancias diferentes (llamadas productos), a través de la ruptura y formación de enlaces químicos entre átomos y moléculas. Durante una reacción química, los átomos se reorganizan para crear compuestos químicos nuevos con propiedades distintas de las sustancias originales.
Las reacciones químicas se representan mediante ecuaciones
químicas, donde los reactivos se sitúan en el lado izquierdo y los productos en
el lado derecho, separados por una flecha. Los coeficientes estequiométricos
indican la proporción en la que los reactivos se combinan y los productos se
forman. Es importante destacar que durante una reacción química, la masa total
de los reactivos es igual a la masa total de los productos, lo que se conoce
como la ley de conservación de la masa.
¿Para que nos sirven las reacciones quimicas?
Las reacciones químicas tienen una amplia gama de
aplicaciones y beneficios en nuestra vida cotidiana, en la industria y en la
investigación científica. Aquí hay algunas formas en las que las reacciones
químicas nos son útiles:
Formulas de Reacciones Quimicas
Las fórmulas de las reacciones químicas se representan utilizando símbolos y fórmulas químicas para describir los reactivos y productos involucrados en la transformación química. Aquí hay una explicación básica y un ejemplo de cómo se escriben las fórmulas de las reacciones químicas:
En una reacción química, los reactivos se encuentran en el lado izquierdo de la ecuación, y los productos se encuentran en el lado derecho. La flecha (→) se utiliza para indicar la dirección de la reacción, es decir, la conversión de reactivos en productos. Aquí está un ejemplo simple de una ecuación química:
Reacción de Combustión del Metano:
CH₄ + 2O₂ → CO₂ + 2H₂O
- CH₄: Fórmula química del metano, un hidrocarburo.
- O₂: Moléculas de oxígeno.
- CO₂: Dióxido de carbono, uno de los productos.
- H₂O: Agua, otro producto.
La ecuación indica que un mol de metano reacciona con dos moles de oxígeno para producir un mol de dióxido de carbono y dos moles de agua. Los números que aparecen como coeficientes antes de las fórmulas químicas se llaman coeficientes estequiométricos y representan las relaciones molares en la reacción. Estos coeficientes aseguran que la ley de la conservación de la masa se cumpla en la reacción, lo que significa que la cantidad total de átomos de cada elemento se mantiene constante antes y después de la reacción.
Es importante recordar que las reacciones químicas deben estar balanceadas, lo que significa que el número total de átomos de cada elemento debe ser igual en ambos lados de la ecuación. El balanceo de ecuaciones químicas es un proceso fundamental en la química para asegurarse de que las relaciones estequiométricas sean correctas y que se respete la conservación de la masa.